新しいくすりを患者のもとへ届けるには長い年月と多額の研究開発費が必要となる。くすりのモトとなる新規物質の発見から基礎研究、非臨床試験、臨床試験(治験)、審査など数多くの段階があり、平均して9〜17年かかる。
その費用も膨大で、かつ増加傾向。'13年の研究開発費は1社あたり約1,400億円だったと、製薬協Webサイトで説明されている。ほかにも、くすりができるまでには約10年の期間と200~300億円のコストがかかるとの話(日本SMO協会)がある。
製薬企業全体では年間1.4兆円を投入する。新薬開発の治験におけるコスト削減が課題となっている。近年、様々な業種でペーパーレス化が進み、医療分野では特に新薬開発プロセスにおいて、製薬企業による電子化への対応が進んでいる。一方、医療機関では治験文書への押印など紙文書による運用が一般的であり、治験期間中に発生する煩雑かつ膨大な紙文書の印刷やファイリング作業、保管スペースの確保も課題だ。
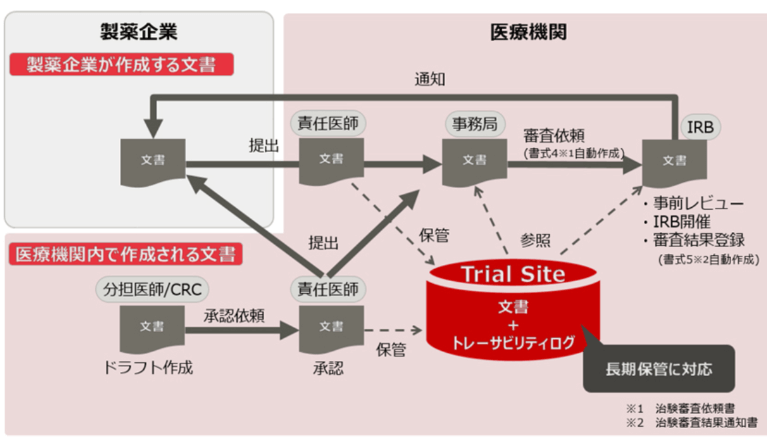
紙文書の授受や保管状況の確認のために直接両者間を行き来する製薬会社の担当者にとっては、治験の工数削減への対応も急務になっているという。富士通は、治験業務を支援する「tsClinical DDworks21」シリーズのラインナップを強化、製薬企業と医療機関との間でやり取りされる治験文書をクラウドで共通管理できるSaaS型ソリューション「tsClinical DDworks21/Trial Site」を24日、国内の医療機関向けに提供開始する。
治験の信頼性を担保・証明する治験文書は、法令により厳格な管理と長期の保管が求められている。その運用を紙でする医療機関では、上述の課題に加え、新薬承認後5年(欧州規制:最低25年)間の適正な管理も現場の負荷になっているという。富士通は、今回のソリューションにより、それら業務の負荷を低減、効率化やコスト削減にも貢献していく構えだ。
