アルファ線がん治療を進展させる、アスタチン-211の標識法を開発」
がんに対する一般的な放射線治療では、X線や電子線といった比較的高エネルギーの放射線を、患者の体外から腫瘍に向けて照射する。また最近、放射免疫療法(放射線内用療法の一種)として、β線やα線放射核種を抗体に標識した「放射性がん標的分子」の開発が行われている。同分子はがん細胞に特異的に結合するため、がん細胞のみへの照射による効率的な治療ができ、周辺組織への損傷リスクを低減できる。
β線核種を標識した90Y標識リツキシマブ(ゼヴァリン)、131I標識トシツモマブ(ベキサール)などが放射性抗体医薬品として実用化されている。そしてより強力で効果が期待される、α線核種を用いた放射線内用療法の研究も進められている。現在、放射性抗体医薬品の作製において、放射性標識反応に用いられる代表的な手法が活性エステル法(スクシンイミジルエステル化合物でペプチドやタンパク質のアミノ基を標識)である。
従来報告されたほとんどのα線核種標識分子が、活性エステル法を利用して合成されている。がしかし、この手法では、実用的な反応効率で標識反応を達成するために、高濃度条件下で生体分子と標識剤を反応させる必要があり、数時間から終夜の長い反応時間も要するという。理化学研究所の田中生体機能合成化学研究室は、理研クリック標識技術と仁科加速器科学研究センターのRI(放射性同位元素)製造技術を用いて、α線放射核種アスタチン-211(211At)の実用的な標識法を開発した。
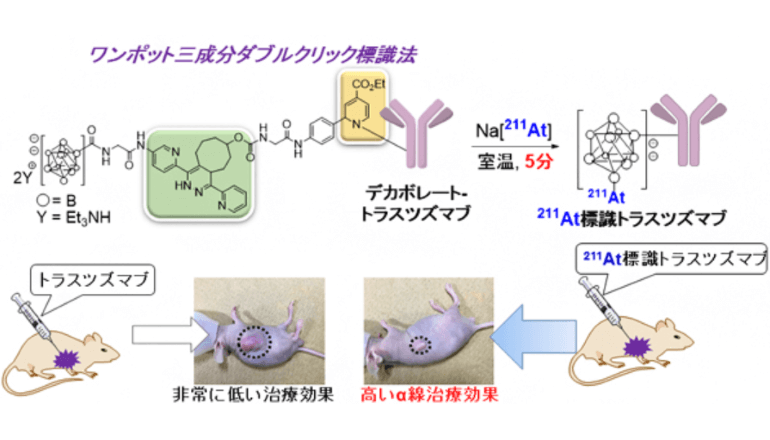
抗がん抗体(トラスツズマブ)に対する放射線がん治療効果が期待されるという。同研究室のグループは、これまでに2つのクリック(シートベルトを締めるように高効率な結合形成)反応――「理研クリック反応(高速6π-アザ電子環状反応)」と「テトラジンライゲーション(逆電子要請型Diels-Alder反応)」を一挙に行い、生体高分子を効率的に放射性標識する「ワンポット三成分ダブルクリック標識法」を開発していた。そして今回、211Atが安定に結合するデカボレート(ホウ素化合物)を導入した「デカボレート-テトラジンプローブ」を開発。
ワンポット三成分ダブルクリック標識法を用いて、加速器サイクロトロンで製造した211Atを、トラスツズマブに効率的かつ簡便に標識することに成功し、さらに、表皮がんマウスの腫瘍内に合成した211At標識トラスツズマブを投与したところ、高いα線がん治療効果を示すことが分かったという。抗体などのさまざまな生体高分子の211At標識に利用することにより、α線がん治療を大きく進展させるだろう。研究成果は、英国王立化学会の科学雑誌『Chemical Science』に掲載された。
