金ナノ粒子を用いた光イメージング技術でがんの生存戦略を明らかに
自らの生存に必要な代謝物を正常組織から収奪し増殖している。中でもグルタチオンやシステイン、硫化水素などの硫黄を含む代謝物は強力な抗酸化物質として、がん細胞の生存、増殖や薬剤耐性などに関与することが示唆されている。が実態は不明であった。
がんの病理診断はおもに染色等の標識を施した組織試料を光学顕微鏡で調べて行われる。細胞の形態や核の特徴に着目した従来手法では、検体処理過程に生じる酸化などが正確な解析を困難にしていた。この分野における、生化学的な自動補助診断技術の開発は、病理医の負担軽減につながるだけでなく、抗がん剤への耐性の有無や悪性度の判定など、患者に資する「質的診断」に役立つ可能性があるという。
慶應義塾大学医学部の研究グループは、AMEDおよびJSTとともに、がんの所在を非標識・無染色で自動的に可視化することに成功したと発表。富士フイルム先端コア技術研究所との共同研究により、表面増強ラマンイメージング(SERS imaging)を用いて、マウス凍結病理組織切片におけるがん部と非がん部の代謝プロファイリング解析を行い、両者の違いを統計的に分析することによって成し遂げたという。
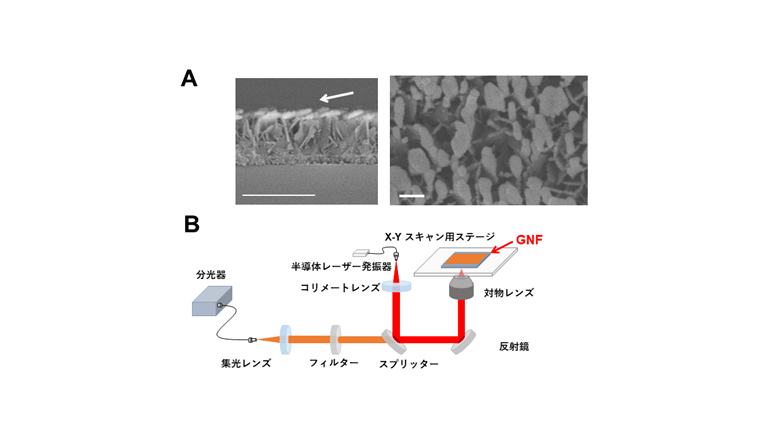
SERS imagingは金のナノ粒子をランダムに敷き詰めた特殊基板に近赤外レーザー光を照射したときに発生する近接場光(電磁場スポット)を利用し、生体試料に含まれる各種代謝物の原子間振動を反映するラマン散乱光を増強して、代謝物の2次元画像として検出する先端技術。
がん細胞には細胞増殖や細胞死の制御に関わる硫黄原子を含有する機能分子が豊富に含まれていて、それらは金ナノ粒子との相互作用によって固有の原子間振動を反映したラマン散乱光を発生させる。この光を画像化することで、生体試料の2次元上に機能分子の存在位置を視覚化できる。
今回の技術を用いて、2つの実験モデルで得られるラマン散乱光のスペクトルピーク(SERS信号)を、がん部、非がん部で詳細に分析――。システインから生成される還元型グルタチオンおよびヒポタウリンを反映するSERS信号を特定したのち、それぞれをがんの診断所見と照合した結果、大腸がん肝転移モデルではがん部にグルタチオンが豊富に検出できる一方、ヒポタウリンはがんの外側の肝臓実質に存在することが分かった。
原子間振動のがん部と非がん部の特徴の違いに基づき、がんの所在を検出できる可能性がある。病理医の診断所見とラマン散乱光のプロファイリング所見のマッチングによる解析技術は、がんの質的自動病理診断の実現への道を開いたという。研究成果は、英国科学誌「Nature Communications」オンライン版に掲載された。
