東京医科歯科大学大学院医歯学総合研究科分子細胞代謝学分野・九州大学大学院医学研究院病態制御内科学分野の小川佳宏 教授と名古屋大学環境医学研究所分子代謝医学分野の菅波孝祥 教授を中心とする研究グループが解明。研究成果は、国際科学誌「JCI Insight」電子版で発表された。
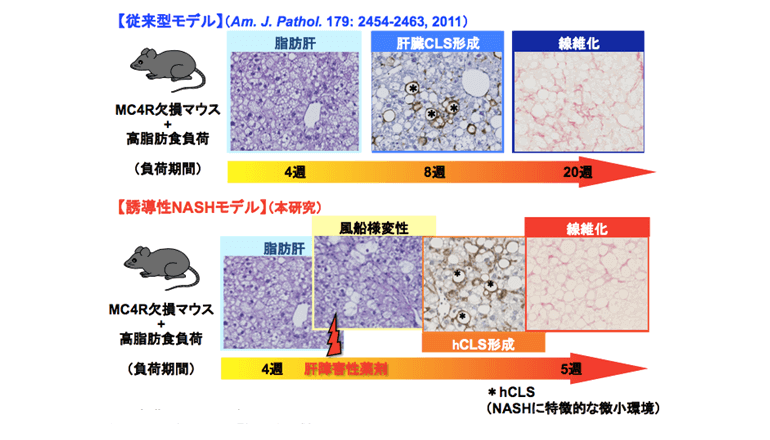
今回、脂肪肝を発症した「MC4R欠損マウス」に肝障害性薬剤投与によって肝細胞死を誘導することで、1週間の過程でNASHを発症する新たな疾患モデル(誘導性NASHモデル)を開発した。NASHの発症に長期間を要する従来型モデルと組み合わせることで、脂肪肝からNASHを発症する過程を詳細に検討することを可能にした。その結果、NASHの発症に先行して、肝臓の局所に特徴的な微小環境(hCLS: hepatic crown-like structure)が形成され、NASHの発症に至ることを見出した。
この微小環境は主に組織常在性マクロファージ(クッパー細胞)で構成され、炎症促進性の形質を獲得することで肝線維化に働くことを明らかにした。マクロファージは白血球の一種で、従来は一様と考えられていたが、近年、臓器や疾患においてそれぞれ特徴的なマクロファージサブタイプが存在し、多種多様であることが明らかになってきた。今回の研究で見出した新たなマクロファージサブタイプは、NASHに特異的なものと考えられるという。さらに、同様のマクロファージサブタイプはヒトNASHにおいても認められ、NASHの病勢を反映することを明らかにした。
今回新たに確立した誘導性NASHモデルは1週間という短期間で肝線維化過程を評価できるため、病態解析や薬剤スクリーニングを効率的に行うことが可能。さらに、この研究結果により、特徴的な微小環境がNASHの発症に重要であることを明らかにした。この微小環境を構成するNASH特異的なマクロファージサブタイプが明らかになったことで、脂肪肝からNASHに進行する病態メカニズムの解明や、新しい治療戦略の開発に役立てられることが期待される。
