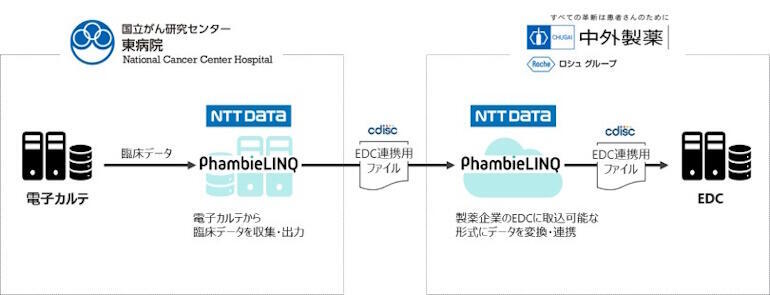
電子カルテから製薬会社のEDC(電子データ取得)に臨床データを連携させる取り組みが注目されている。それはしかし互換性や製品の違い等のため普及しておらず、中でも、安全性評価で重要な有害事象や併用薬情報についてのデータ連携の取り組みは極めて稀だ。
新薬開発は研究や治験での臨床データの収集・解析、有効性と安全性の評価等のプロセスを経て9~17年程度かかる(出典:製薬協)。製薬会社・医療機関双方で多大な労力と時間が費やされる臨床データの収集では、業務効率化と品質確保が課題となっている。臨床データの連携は対象の拡充が求められているという。
国立がん研究センター東病院、中外製薬とNTTデータは昨年6月~今年1月、電子カルテに記載された臨床データのEDCへの連携に関する共同研究を実施した。PhambieLINQを活用し、疾患領域を限定せず、有害事象・併用薬を含めて、治験で必要となる主要な臨床データの連携を可能とした。
ⅰ.電子カルテからEDCへの電子的な連携は、オペレーションおよび信頼性(データ品質等を含む)の観点から実試験での利用可能性があることを確認――。有害事象36%、併用薬73%、患者背景18%、バイタルサイン63%、臨床検査値86%の連携を達成した。
ⅱ.データ連携により、①EDCシステムからの自動配信クエリは1例あたり11件中6件に。マニュアルクエリは同9件中2件に削減。②医療機関の転記作業については1例あたり1時間程度――、製薬企業のSDV(元データ検証)作業については同1.5時間程度の削減効果を認めた。医療機関のEDC入力にかかる心理的負荷の軽減への寄与も確認した。
今回の結果は世界的に見ても先進的な事例であり、治験業務のデジタル化を前進させるものだという。3者は、医療機関と製薬会社の治験業務効率化・高品質化を実現し、新しい医薬品が1日でも早く患者に届くように貢献していく構えだ。
