糖鎖とは、単糖であるマンノースやシアル酸などが数個以上、枝分かれしながら結合した物質。タンパク質を構成するアミノ酸の一つであるアスパラギンに結合する糖鎖は「N結合型糖鎖」と呼ばれ、細胞ががん化するなど病変する際には、この糖鎖の構造が変化することが知られている。このような疾患特異的に変異する糖鎖を標的とした医薬品を開発できれば、これまでよりも副作用が少なく効果の高い画期的な治療を実現できると期待されている。
病変細胞を採取して解析する場合、まず組織切片を染色して顕微鏡で観察しながら病変細胞を切り取るが、多くの場合1,000細胞未満のわずかな量しか得ることができないという。高感度なN結合型糖鎖分析法として知られる「キャピラリー電気泳動-レーザー励起蛍光(CE-LIF)分析法」であっても、最低でも10,000細胞以上の試料が必要であり、病変細胞のみを糖鎖分析にかけられなかった。
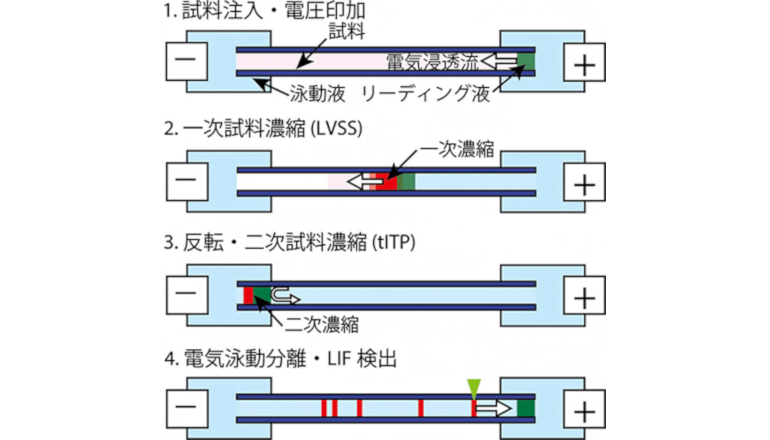
今回、共同研究チームは、高感度な糖鎖分析法として知られる「キャピラリー電気泳動-レーザー励起蛍光(CE-LIF)分析法」において、糖鎖を2,000倍以上濃縮できる「新しい濃縮法(LDIS法)」を開発し、検出下限濃度350fmol/L(フェムトモーラー、1,000兆分の1モル濃度)という超高感度を実現した。
研究グループによると、東京ドーム3杯分の水に対して角砂糖1個分に相当。LDIS法は、これまでの濃縮法では排除できなかった、不純物による悪影響をほとんど受けない優れた特性があるという。これにより、100細胞という超微量の細胞から抽出された糖鎖をほとんどロスすることなく、濃縮・分離・検出することに成功したと説明する。
研究成果は、これまで検出が難しかった微量血中糖鎖を用いた次世代がん診断や、細胞数の少ない初期がんや難治性がんなどを対象とした創薬に貢献すると期待できる。国際科学雑誌『Journal of Chromatography A』電子版(2018年6月23日)に掲載された。
