東京大学分子細胞生物学研究所の厚井悠太大学院生、木戸丈友助教、宮島篤教授ら研究グループが成功。研究成果は7月28日、米科学誌「Stem Cell Reports」電子版に掲載された。
代謝や解毒、恒常性の維持などの機能を有する臓器である肝臓は、多彩な肝機能を実質的に担う「肝実質細胞」(肝細胞)と「肝非実質細胞」(肝類洞内皮細胞、肝星細胞など)から構成される。
特に、肝細胞は種々の代謝酵素を発現し、肝機能の中心を担うことから、創薬研究や再生医療研究への応用を目的として、近年ヒトiPS細胞から肝細胞を誘導する試みが活発に行われている。しかし、肝非実質細胞の分化・成熟過程には未だ不明な点が多く残っていた。
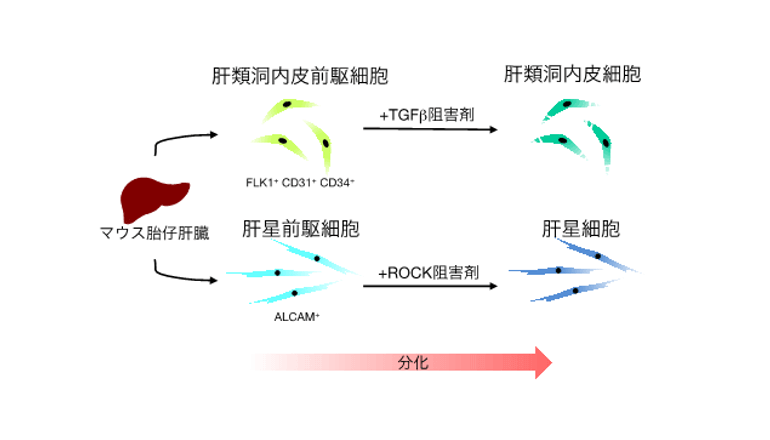
研究グループは、ヒトiPS細胞から肝臓の毛細血管を構成する「肝類洞内皮細胞」、肝類洞内皮細胞と肝細胞の間にある「肝星細胞」の分化誘導系を新たに開発することを目指し、まずマウス肝発生過程における肝非実質細胞の「前駆細胞」の同定とその増殖、成熟化培養系の樹立を行った。肝類洞内皮細胞、肝星細胞の分化には、それぞれ「TGFβシグナル」「Rhoシグナル」が関与することを見いだした。
樹立とは、生体から単離した細胞や遺伝子などに何らかの手を加えた細胞を安定的に培養し、医学や生物学の研究に利用できる状態にすることを指す。
また、研究グループは各非実質細胞の前駆細胞の分離法や増幅・成熟化培養系をヒトiPS細胞から細胞を機能的に変化させること(分化誘導)に応用。ヒトiPS細胞由来の肝前駆細胞、肝類洞内皮細胞、肝星細胞を用いたヒト肝臓モデルの構築に成功し、60種類の肝代謝マーカーの発現が顕著に増加することを明らかにした。
今後は、構築したヒト肝臓モデルを肝炎ウイルスの感染など肝疾患モデリングへ応用し、新たな予防・診断・治療薬の開発を目指す。
